慶應義塾大学(慶応大)は、紫外線や放射線、加齢などによって細胞に蓄積する「活性酸素」の細胞毒性を逆手に取った新たながん治療戦略を見出したと発表した。
成果は、慶應大の久保田義顕特任講師、奥野祐次研究員らの研究グループによるもの。研究の詳細な内容は、米国東部時間7月15日付けで英科学誌「Nature Medicine」オンライン版に掲載された。
活性酸素は酸素分子がより反応性の高い化合物に変化したものの総称だ。一般的には、「スーパーオキシドアニオンラジカル」、「ヒドロキシルラジカル」、「過酸化水素」、「一重項酸素」の4種類とされる。
活性酸素は細胞が呼吸する際に常に細胞内で発生し続けており、紫外線や放射線、加齢などによりさらに細胞に蓄積してしまう。活性酸素は細胞内のさまざまな物質に対して有害な化学反応=細胞毒性をもたらし、細胞に損傷を与える。その結果、老化現象、動脈硬化や糖尿病などの生活習慣病、がんなどさまざまな病気の原因となるのだ。
それに対し、各細胞内には通常、「高酸化酵素」と呼ばれる、活性酸素を消去する酵素(抗酸化酵素)として「カタラーゼ」や「スーパーオキシドディスムターゼ」、「ペルオキシダーゼ」などが存在し、活性酸素による細胞の障害を防いでいる。
活性酸素は以上のような体内における問題のある物質な分だが、その一方で少量の活性酸素は細胞増殖・生存のシグナルとして働き、ヒトの体と活性酸素の関係においてよい面も存在するという事実も指摘されてきた。
今回の研究は、活性酸素のがんの進行に対して与える影響が、実際のところよいものなのか悪いものなのかを明確にすべく、特にがんに栄養を送る重要な役割を担う「新生血管」に焦点を絞って考察が行われたのである。
がんの増大には、それに見合う新生血管による血管網の成長が必要だ。がん新生血管に限定的に強く発現する遺伝子を網羅的に解析した結果、活性酸素を消去するために重要な役割を果たす「Atm(毛細血管拡張性肉芽腫変異)遺伝子」が活発に働いていることが見出された。前述した抗酸化酵素を制御しているのが、Atm遺伝子である。
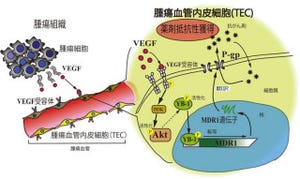
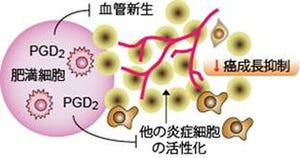
そこで研究グループは、Atm遺伝子が血管細胞において欠損する遺伝子改変マウスを作製。すると、同マウスの皮下に移植したがん(悪性黒色腫)の新生血管において、Atm遺伝子の活性酸素を消去する作用がないため、活性酸素が過剰に蓄積し、血管の早期老化退縮が誘導されるのが確認されたのである。その結果、本来はがんに酸素・栄養を供給するべき血流が乏しく、がんの増殖が著明に抑制されたことがわかったというわけだ(画像1・2)。
|
|
|
|
Atm遺伝子欠損によるがん増殖抑制メカニズム。画像1(左)は通常のがん、画像2はAtm遺伝子欠損マウスのがんの模式図。通常のがんではAtmタンパクの活性により活性酸素が消去され、がんに栄養を送る血管が成長可能だ。しかし、Atm遺伝子欠損マウスでは、Atmタンパク質の活性酸素消去作用が働かないため、がん新生血管で活性酸素が過剰蓄積し、早期老化退縮し、これによりがんの増殖が抑えられるという仕組みだ |
|
研究グループは現在、Atm遺伝子の活性酸素消去作用を特異的に阻害する化合物を開発中だ。同化合物はがんの新生血管にのみ得意敵に活性酸素を蓄積させることが可能であり、正常組織にダメージの少ない新たながん治療を切り開けるものと期待されるとしている。