東京大学(東大)は、幼若時に熱性けいれんを生じたラットが成長後にてんかんを発症することを見出し、さらに、その原因が「未熟な海馬に発作が生じると神経回路の発達が障害され、この異常が成人まで残る」ことであると突き止めたほか、実際に薬を使って海馬の発達障害を防ぐことで、てんかんを予防することができることを確認したと発表した。同成果は同大大学院薬学系研究科の小山隆太 助教と池谷裕二 准教授らの研究チームによるもので、英国科学誌「Nature Medicine」オンライン版に掲載された。
熱性けいれんは発熱中に起こり、乳児および小児が経験するもっとも一般的なけいれん発作として知られている。熱性けいれんには単純型と複雑型があるが、単純型の予後は良好ながら、複雑型は将来、側頭葉てんかんへと発展する危険があることが臨床上よく知られている。しかし、この現象の因果関係についての厳密な証拠はこれまでなく、また、メカニズムも知られていなかった。
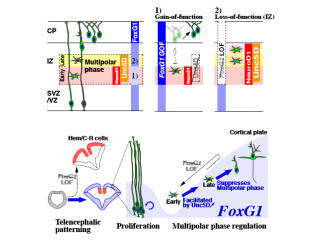
側頭葉てんかん患者の海馬では、神経細胞の過剰同期発射を生じやすい神経回路の異常が生じている。一方、熱性けいれんを経験する幼若期は、神経回路の発達の時期と一致しており、このことから研究チームは「熱性けいれんが、回路の発達異常を引き起こし、てんかん発症へとつながる」と推察。熱性けいれんがどのように顆粒細胞の移動に影響を与えるのかを明らかにすることで、てんかんの発症メカニズムの解明を試みようと研究を行った。その結果、乳幼児期の脳の生じる現象を詳らかにするためには、従来のような固定されたヒト脳標本を観察するアプローチだけでは不可能であるとの結論から、今回、緑色蛍光蛋白質(GFP)発現ラットに熱性けいれんを誘導し、および新規に同モデル由来の海馬切片と野生型ラット由来の海馬切片を組み合わせて培養する技術を開発、熱性けいれんの影響を受けた細胞の挙動を可視化すること成功した。
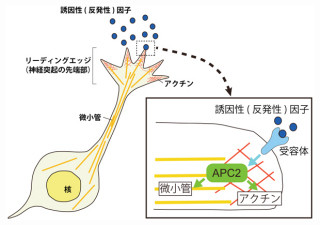
その結果、熱性けいれんの影響を受けた顆粒細胞は、運動方向に異常をきたし、本来到達すべき正常な標的まで移動できず、異所的に配置されることを確認。この分子メカニズムとして、熱性けいれんの影響を受けた顆粒細胞では、GABAA受容体の発現が上昇しており、GABAによる興奮を受けやすくなっていることを発見した。また、GABAによる興奮が引き起こすCa2+の細胞内流入が、移動異常の原因であることも明らかにした。
さらに、移動中の顆粒細胞に対してGABAが興奮性に働く原因は、GABAによる神経興奮性作用と、この作用を担うNKCC1共輸送体が関与することをつきとめたほか、NKCC1共輸送体の阻害薬であるブメタニドを熱性けいれん後に連投することで、異所性顆粒細胞の出現を抑え、将来のてんかん発症を抑制することに成功したという。
今回の研究結果は、熱性けいれんと将来のてんかん発症に関して、乳幼児期におけるGABAの興奮性作用が関与するという新知見を与えるもので、GABAの興奮性作用を担う分子であるNKCC1共輸送体をターゲットとした、新規のてんかん予防法を提案するものとなった。また同時に、GABAを活性化させる従来の熱性けいれんの治療法は、短期的にけいれん抑制効果があるものの、長期的にはむしろ、てんかんの危険性を高めてしまう可能性が指摘された。
加えて、今回の成果は、乳幼児期の経験が将来の脳機能へおよぼす影響をどう検証していくか、という重要なテーマに新たな研究手法を提案するもので、こうしたアプローチを活用することで、脳疾患における細胞・分子メカニズムの解明が進み、さらなる創薬につながることが期待されると研究チームではコメントしている。