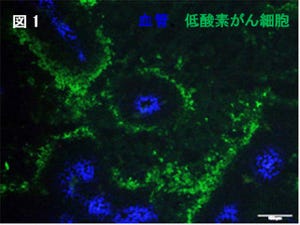
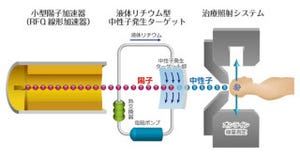
放射線医学総合研究所(放医研)は6月4日、高線量の放射線をラットの「胸腺細胞」に当てると細胞死が誘導されて細胞サイズが縮小する現象を利用して、放射線防護効果を迅速・簡便・低コストでスクリーニングできるアッセイ法を確立したと発表した。
成果は、放医研 重粒子医科学センター 国際重粒子医科学研究プログラムの関根(鈴木)絵美子研究員、同センター 先端粒子線生物研究プログラムの松本謙一郎チームリーダー、下川卓志チームリーダー、中西郁夫主任研究員、上野恵美准研究員、日本薬科大学物理系薬学分野の安西和紀教授らの共同研究グループによるもの。
今回の手法法は、「スクリーニング方法、スクリーニングキット、及び解析プログラム」として、2012年3月27日に特許出願され、6月7日・8日に徳島県で開催される「第65回日本酸化ストレス学会」で発表される。
放射線がん治療は欧米ではすでにがん治療の第1選択肢となっており、近年、日本でも放射線がん治療が増える傾向にある。がん周囲の正常組織の炎症など、放射線による副作用を効果的、効率的に予防できれば、さらに放射線治療の普及が進むものと期待され、正常組織を放射線から防護できる効果的な「放射線防護剤」の開発は放射線治療の高度化に重要であると考えられる。
しかし、放射線防護剤の従来のスクリーニング方法は、時間や手間、費用がかかるという問題があり、開発の大きな阻害要因となっていた。
放射線防護剤の研究はこれまでにも多数行われてきたが、副作用が強いことなどから実際に臨床現場で応用されているものはほとんどない。その候補化合物は多く存在するが、従来の放射線防護効果の評価法では、評価に必要な化合物の量が多い、試験期間が比較的長い、実験操作が煩雑である、コストがかかる、技術習得まで時間がかかるといった問題点の1つ以上を有していたため、多種類の化合物のスクリーニングには不向きだった(画像1)。
|
|
|
画像1。今回開発された手法と従来法の比較一覧表。「実験動物の生存率測定」のコスト8万円の根拠は、マウスを使用した場合1匹2000円程度。コントロール、試料のみ、放射線のみ、試料と放射線の4群比較で、1群n=10として、2000円×40匹=8万円 |
そこで研究グループは、これらの問題点をすべて解決できる手法を開発することを目的として、新しいスクリーニング法を確立した。今回の手法は、放射線でラット胸腺細胞に細胞死が誘導されて細胞サイズが縮小する現象を利用して、対象化合物の放射線防護効果を判定できるスクリーニング法だ。
そして、従来法と比べて非常に時間と経費を抑えたアッセイであり、新薬などの毒性判定等に一般的に使われる「コメットアッセイ」や「MTT アッセイ」と比較して時間もコストも半分以下となる(画像1)。今回の手法を初期的なスクリーニングとして用い、その結果を基に従来の方法を併せて検討することで、新薬開発の加速化が期待される。
ラットから摘出した胸腺細胞を「10%ウシ胎児血清添加RPMI1640培地」に懸濁し実験に使用する(ラット1匹から2000~2万試料を試験できる大量の胸腺細胞が得られる)。
この胸腺細胞にX線を照射し数時間培養すると、胸腺細胞の縮小、核の濃縮が観察される。ここで、染色することなく細胞の大きさを「フローサイトメトリー」や「セルカウンター」で検出する点が簡便化の1つだ。
また、培養細胞株などのように細胞が断片化してできるアポトーシス(細胞自死)小体を形成するのではなく、細胞が断片化せず凝縮する性質を利用することで、死細胞の割合を正確に検出することが可能になる。
胸腺細胞は感受性の高い正常細胞であり、このような反応が数時間で起こるので、細胞の縮小が一定して起こる初期の反応に注目することで、短時間での測定・評価が可能となった。
また、培養細胞株と違い継代中の性質の変化がなく、摘出した胸腺細胞の細胞周期がそろっていることにより細胞周期の依存性の問題がないため、精度がよく再現性の高いスタンダードな方法として使えるとしている。
画像2は実際のスクリーニング結果を説明するグラフで、横軸が細胞サイズを、縦軸が細胞数を示している。この実施例では、(A)未処理の胸腺細胞(非照射、薬剤添加無のコントロール)、(B)X線2Gyの照射、(C)「カテキン誘導体」1mMの添加、(D)カテキン誘導体1mMの事前添加とX線2Gyの照射が行われた。
X線2Gyは一般的な放射線治療で、照射を何日かに分割した場合に1日に照射する量だ。処理後ただちに5%CO2存在下で37℃で4時間培養し、細胞サイズをフローサイトメトリーの1種「FACSCalibur」(BD社製)で測定した。今回の実施例において生細胞ピーク位置をL(L1~L4)、死細胞ピーク位置をA(A1~A4)と表示している。
画像2(A)の未処理細胞では、細胞の大きさのピークは400付近、(B)のX線2Gyを照射した細胞では、大きさのピークは200付近となっている。この結果により、胸腺細胞に2Gyの放射線を照射すると細胞が凝縮し、細胞サイズがおよそ半分になることがわかる。
(D)はカテキン誘導体1mMを事前投与して(B)と同じ処理をした胸腺細胞だが、(B)とは違い、ピークが400付近(生細胞ピーク位置L4)のままであり、カテキン誘導体の放射線防護効果を示唆していることがわかる。
今回の手法は放射線のみならず、胸腺細胞に細胞死を誘導するような細胞障害性因子であれば判定が可能であるため、新薬や新規化合物の毒性判定においても利用できる。今回の手法により、放射線防護剤以外にも放射線増感剤、薬剤の毒性、薬剤の使用条件(薬剤濃度、投与形態)などもスクリーニング可能だ。
また今回のスクリーニング法は、全工程における実験操作が容易であり、明瞭で再現性が高く精度のよい客観的な結果を短期間で安価に得ることができ、非常に効率的なアッセイである。
さらに、一般的な大学・研究施設等で所有しているフローサイトメトリーなどを用いて測定できるため、今回の手法は多くの研究現場でコストをかけずに利用することが可能だ。
なお研究グループは、より多くの放射線を患部に照射することで、がん組織に対する治療効果を向上させ、総合的にがん治療を高度化することを目指している。
その一環として、がん組織の周りにある正常組織が放射線によって障害を起こすのを防止する放射線防護剤に着目し、候補化合物となりうる種々の「新規抗酸化物質」を、天然抗酸化物質を化学修飾することにより開発してきた形だ。
今後は、これらの化合物に対し、上記のスクリーニング法を用いて放射線防護効果の評価を行うと共に、各化合物の化学構造に基づく機能解析及び分類、構造活性相関を検討し、有効性が高く臨床応用可能な新しい放射線防護剤を開発していく予定だ。