産業技術総合研究所(産総研)は3月27日、ヒト細胞核中の「U7核内低分子RNA(U7 RNA)」が、細胞内の状態に応じて、2つの相反する遺伝子発現制御を行うことを発見したと発表した。成果は、産総研バイオメディシナル情報研究センター機能性RNA工学チーム廣瀬哲郎研究チーム長、同細胞システム制御解析チーム夏目徹研究チーム長らの研究グループによるもの。研究の詳細な内容は、「米国科学アカデミー紀要(PNAS)」に掲載の予定。
ヒトゲノム解析によって、ヒトのタンパク質遺伝子の数が、マウスのものとほとんど変わらないことが判明した。そして「ポストゲノム研究」によって、ヒトゲノムやマウスゲノムの大部分から、機能のわからないRNA(リボ核酸)が多数生産されていることも明らかになった。
RNAには多くの種類があり、たとえば全RNA量の80%を占める「リボソームRNA(rRNA)」やDNAの遺伝情報がコピーされた「メッセンジャーRNA(mRNA)」、アミノ酸を運ぶ「トランスファーRNA(tRNA)」、酵素の働きを持つ「リボザイム」などがある。
RNAの内、こうしたmRNAやtRNAのように機能を持つRNAのことを総称して「機能性RNA」と呼ぶ。DNAの遺伝情報に基づいて生体内でタンパク質が合成されるためには、実際にはこうしたさまざまなRNAによる両者の間の仲介が必要となる。
ゲノム配列の決定を受けて、ゲノム機能解明を指向した一連の分子生物学/医学研究が行われるようになったのだが、それらを総称してポストゲノム研究と呼ぶ。ゲノムから合成されたRNAを網羅的に解析する「トランスクリプトーム解析」などは、ポストゲノム研究の1つである。
ちなみにトランスクリプトーム解析に関しては、「完全長cDNA」(ゲノムから取り出したmRNA(メッセンジャーRNA)の塩基配列情報を完全に写し取った相補鎖DNA)配列の大規模解析が産総研、理研グループによって行われ、先駆的な成果が得られた。
ヒトとマウスにおいて実施され、7割以上というゲノム中の大部分が転写されRNAが産生されていることが明らかになっている。その後高速シーケンサーの出現により、その解析精度が飛躍的に向上した。
ポストゲノム研究が進む中、機能不明のRNAについても徐々にわかってきたことがある。それらはタンパク質のアミノ酸配列をコードしない(翻訳する情報を含まない)ことから、「ノンコーディングRNA」と呼ばれている。
タンパク質へと翻訳されずにRNA自身で働く機能性RNAであり、働く場は主に細胞核内においてと目されている。ちなみにポストゲノム解析によって数1000種類に上るノンコーディングRNAが見出されたが、ほとんどの場合その機能は不明だった。
しかし、最近になってそうしたノンコーディングRNAの一部が、遺伝子発現の制御や細胞内構造形成、さらには疾患の発症にかかわることが明らかにされ、RNAの制御機能に注目が集まってきている。
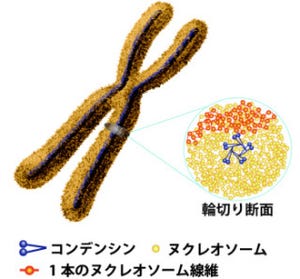
DNAに結合して染色体を構成するタンパク質「ヒストン」(酸性のDNAとは高い親和性を示し、約146bpのDNAは八量体のヒストンに1.65回巻き付く)は塩基性が強く、結合するDNAがなくて単独となった過剰なヒストンは、細胞にとって有害である。
そのためヒストンの遺伝子は、細胞内のDNA複製時期(S期)にだけ発現するように厳密に制御され、細胞核内で新しい染色体が形成されるS期にのみヒストンが合成される仕組みだ(画像1・中)。
細胞核内に局在するU7 RNAは、ヒストン遺伝子の「mRNAプロセシング」を促進することによって、S期のヒストン合成に寄与している(画像1・左)。mRNAプロセシングとは、核内で行われるmRNAの成熟化段階をそう呼ぶ。
真核生物では、細胞核内でDNAから転写された「前駆体mRNA」がさまざまな加工(プロセシング)を受けて「成熟型mRNA」になり、その後に細胞質に輸送されて翻訳される。前駆体mRNAからのイントロン領域の除去のためのRNAスプライシングや、mRNAの分解を防ぐためにRNA両末端にキャップ構造やポリA鎖が付加される現象も含まれる形だ。
一方、U7 RNAは、S期以外のDNA複製が起こっていない時期にも豊富に存在していることが知られていた。今回、S期以外の細胞を用いて、U7 RNAだけを、「アンチセンス核酸」によって分解したところ、通常なら発現が抑制されているヒストン遺伝子の転写が著しく上昇したのである。
またU7 RNAを過剰に細胞内で合成させると、逆にヒストン遺伝子の転写を抑制することに成功した。これらの結果からS期以外の細胞では、U7 RNAはヒストン遺伝子発現を抑制し、余分なヒストンを作らないように制御していることがわかったのである(画像1・右、画像2)。
ちなみに、アンチセンス核酸とは、RNAの標的配列に対になる配列(相補的配列)を持つ1本鎖DNAのことを指す。細胞の「RNaseH活性」を利用して、1本鎖DNAと結合した標的RNAを特異的に分解することができる。ただし1本鎖DNAは細胞内で不安定であるために、分子骨格を化学的に安定なものと入れ替えたものを用いる場合が多い。
|
|
|
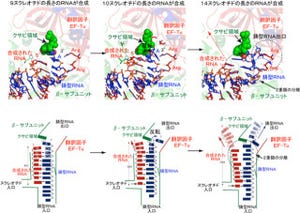
画像2。U7 RNAの2つの機能によるヒストン遺伝子発現制御。「*」はヒストンmRNAプロセシング促進機能、「**」はヒストン遺伝子転写抑制機能が働いていることを示す。「+」は発現・DNA複製・hnRNPUL1タンパク質の機能があることを指し、「++」は特にそれが強い意味を表す。「-」はそれらがないことを示している |
ヒストン遺伝子発現を抑制するため、U7 RNAは特異的なタンパク質と複合体を形成していると考えられた。そこで、U7 RNAに結合しているタンパク質を高感度質量分析によって探索した結果、「hnRNPUL1」タンパク質を新たに同定することに成功した。
hnRNPUL1は、哺乳類の細胞核内に比較的豊富に存在するRNA結合性タンパク質の1種だ。推定分子量96キロダルトン(96000)、856アミノ酸からなる。RNA結合ドメイン以外にDNA結合性ドメインも持つことから、RNAとDNAの両方に結合する可能性が指摘されている。またアデノウィルスタンパク質、エピゲノム制御因子、転写因子と相互作用し、転写制御やDNA修復制御などにかかわるという報告例がある。
hnRNPUL1タンパク質の機能阻害実験、過剰発現実験を行ったところ、U7 RNAの機能解析と同様に、ヒストン遺伝子の転写を制御することが確認できたというわけだ。
また、hnRNPUL1タンパク質が抑制機能を発揮するには、U7 RNAが必要であることも確認された(画像1・右、画像2)。一方、hnRNPUL1タンパク質の機能を阻害しても、U7 RNAによるS期のヒストン合成は影響を受けいことを確認。U7 RNAの転写抑制機能のみに異常が現れたことから、このhnRNPUL1タンパク質は、U7 RNAの転写抑制機能だけに関与するタンパク質因子であることがわかった(画像2)。
このように、U7 RNAは、S期にはヒストン合成を促進し、S期以外にはヒストン合成を抑制するという2つの重要な役割を担っていることが判明。研究グループは、こうしたRNA機能を利用することにより、発現強度を段階的に調節できる人工遺伝子スイッチの開発などの応用が期待されるとした。
U7 RNAの2つの機能のメカニズムの詳細を解明する。さらに、どのようにして細胞状態を感知して機能を転換できるのかを明らかにする予定だ。また、ヒストン遺伝子以外のU7 RNAの標的を探索/同定することも目指すとしている。