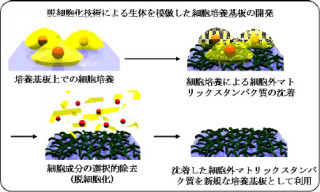
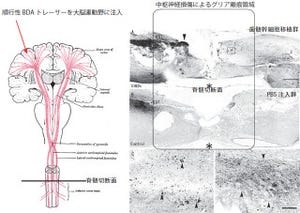
東北大学は、人工多能性幹細胞(iPS細胞)から、エナメル質を作る「エナメル芽細胞」の誘導に成功したと発表した。研究は東北大学病院の新垣真紀子医員、歯学研究科の福本敏教授らと、米国国立衛生研究所、岩手医科大学、東京理科大学の共同研究グループによるもので、成果は米科学雑誌「The Journal of Biological Chemistry」電子版に掲載された。
歯はエナメル質、象牙質、セメント質の3つの硬い組織から成り立っている。この中で、エナメル質は生体内で最も硬い組織であり、人が食生活を営む上で重要な役割を持つ。これまでエナメル質は、一旦齲蝕(むし歯)などで破壊されると、再生させることは不可能であり、人工物による修復しかできなかった。そこで、エナメル質を作るエナメル芽細胞の培養や、その分化制御法の開発が望まれていたのである。
象牙質を作る象牙芽細胞やその前駆細胞は、一生涯歯の中の「歯髄」(歯の神経)に存在し続けるが、エナメル芽細胞は、歯が萌出する(生える)と体の中には存在しない細胞となってしまう。そのため、エナメル芽細胞の分化機能の解明や、歯の再生技術開発のためには、マウスの胎児組織を用いた方法しか存在していなかった。
また、歯は「歯胚」と呼ばれる小さな原基から形成される。この歯胚は口腔内の上皮細胞「歯原性上皮細胞」と、「神経堤」由来の「間葉細胞」との相互作用「上皮-間葉相互作用」により形成される仕組みを持つ。そしてその相互作用は、主に相互の細胞から分泌される「細胞増殖因子」や「基質」により行われ、器官の概形や大きさの決定重要であると考えられている。
そこで、研究グループでは、歯の発生メカニズムを解明する目的で、この歯原性上皮細胞とさまざまな幹細胞とを相互作用させることで、幹細胞がどのような運命をたどるのかを解明することに挑んだ次第だ。
その相互作用を見るため、iPS細胞、「歯髄幹細胞」、「歯髄細胞(MP細胞、既に分化している細胞)」の3種類の細胞が用いられた。歯髄幹細胞はSP細胞とも呼ばれ、歯髄の中に0.2~1.0%の割合で存在している幹細胞のこと。この細胞は、神経細胞や骨芽細胞、象牙芽細胞、脂肪細胞などのさまざまな細胞に分化することが可能であり、再生医療への応用が期待されている。今回の研究では、マウス由来歯髄細胞を不死化し、「ヘキスト色素」を細胞に取り込ませた後、色素の排出量の高い細胞集団を、細胞ソーティングを用いて作製した細胞株が用いられた。
ラットの歯胚由来の歯原性上皮細胞株「SF2-24細胞」を敷石状に培養した上に、マウス由来iPS細胞を撒くと、iPS細胞はSF2-24細胞上で、細胞が凝集した小さな塊を形成(画像1)。この細胞塊は、それぞれの細胞と細胞の間が不明瞭な細胞塊である。培養を6日間継続すると、この細胞塊の周囲から細胞の境界が明瞭な細胞が形成され(画像2・左)、さらに培養後10日目では、伸び出してきた細胞は上皮細胞に類似した敷石状の形態を有していた(画像2・右)。
|
|
|
|
画像1。SF2-24細胞は、敷石状の細胞形態を有する。この際棒状に、マウス由来iPS細胞を培養すると、円形の細胞塊を形成。画像2(左)。2種類の細胞を6日間培養すると、人工多能性幹細胞の周囲から細胞の協会が明瞭な細胞が伸び出した。画像2(右)。共培養後10日目では、iPS細胞から伸び出してきた細胞は、上皮細胞に類似した細胞形態へと変化した |
|
SF2-24細胞とマウス由来iPS細胞との共培養の結果、iPS細胞におけるエナメル芽細胞の分化マーカーの「エナメル基質」(エナメル質の形成に関わる細胞外基質(マトリックス)の総称で、代表的な分子として、「アメロジェニン」、「アメロブラスチン」、「エナメリン」などがある)の発現を「RT-PCR法」にて確認した結果、アメロブラスチン、エナメリンの発現が経時的に増加することが見出された(画像3)。また、上皮細胞分化の指標である「p63」や「サイトケラチン14」の発現増加も認められている(画像3)。
そこで、iPS細胞の細胞塊から伸び出してきた細胞集団が、エナメル芽細胞の分化マーカーを発現しているのかどうかを、「抗アメロブラスチン抗体」を用いた免疫染色で確認した結果、iPS細胞の約95%がアメロブラスチン陽性細胞となっていた(画像4)。
また、同様の方法で歯髄幹細胞、歯髄細胞をSF2-24細胞と共培養すると、歯髄幹細胞は「象牙質シアロリンタンパク質(DSPP)」を発現する細胞に分化したが、歯髄細胞はまったく分化しないことが判明(画像5)。なおDSPPとは、象牙芽細胞マーカー分子の1つであり、タンパク質合成後に「象牙質シアロタンパク質(DSP)」と「象牙質リンタンパク質(DPP)」に分解され、象牙質形成に関わる。
|
|
|
画像5。(A)SF2-24細胞と歯髄幹細胞を共培養すると、歯髄幹細胞は象牙質シアロリンタンパク質陽性の細胞へと分化する。(B)一方、SF2-24細胞と歯髄細胞を共培養すると、歯髄幹細胞は象牙芽細胞やエナメル芽細胞には分化しない。(C)SF2-24とマウスiPS細胞を共培養すると、アメロプラスチン陽性の細胞へと分化する |
今回の成果により、SF2-24細胞と共培養を行うことでマウス由来iPS細胞をエナメル芽細胞へ分化誘導することが可能となったという次第だ。
これまでにも、福本教授は岩手医科大学の原田英光教授の研究グループとの共同研究により、マウス由来iPS細胞から、象牙質を形成する象牙芽細胞の分化誘導に成功している。そして今回得られた細胞との組み合わせにより、福本教授は、全身のどこの細胞からも歯を作り出せる可能性が生まれたと考えられるとコメントした。
また、今後はiPS由来の歯関連細胞から、歯を形成しうるかどうかの検討を行うとともに、今までブラックボックスであったエナメル芽細胞の分化メカニズムや機能評価、さらにはエナメル質再生に関する研究へと発展させたいと考えているとしている。