研究チームによって開発された近視モデルマウスは、ヒトで見られる近視と同様に眼軸長が伸び、強膜が薄くなっていることが特徴だという。そのモデルマウスの強膜を透過型電子顕微鏡を用いて観察したところ、近視強膜の線維芽細胞では、「粗面小胞体」の膨張が観察されたとする。これは小胞体の中に、折り畳み不全のタンパク質が蓄積したときに認められる所見で、この状態は「小胞体ストレス」と呼ばれているとする。
ただし、この結果だけでは、近視になったから小胞体ストレスが生じているのか、それとも小胞体ストレスが生じるから近視になるのか、因果関係が明らかではなかったことから、研究チームでは、タンパク質の正常な高次構造形成を促進することで、小胞体ストレスを減弱させる低分子化合物(ケミカルシャペロン)「4-PBA(4-phenylbutyric acid)」を近視誘導時に点眼投与し、近視が抑制されるかどうかの検討を行ったという。
その結果、4-PBA点眼群では、4-PBAを含まない溶媒のみを点眼した対照群と比較して、小胞体ストレスの指標となる小胞体ストレスのマーカータンパク質の活性化が認められなかったほか、点眼する4-PBAの濃度が高いほど、近視の指標である眼軸長(長ければ近視)の伸長と屈折度数(マイナスになると近視)の低下が抑制されることを確認。この抑制効果はほかのケミカルシャペロンでも同様に認められたという。
例えば薬剤「ツニカマイシン(Tm)」は、小胞体機能を担う酵素を阻害することで、実験的に小胞体ストレスを誘導することが可能なことが知られており、今回の点眼投与によって、強膜小胞体ストレスが一過的に誘導できることが見出されたという。
これらを踏まえ、強膜小胞体ストレスを誘導することで近視化が生じるかの検討が行われたところ、非投与眼と比較して、Tm投与眼では眼軸の伸長ならびに屈折度数の低下が認められ、強膜小胞体ストレスの誘導により近視が生じていることが示されたとする。
-
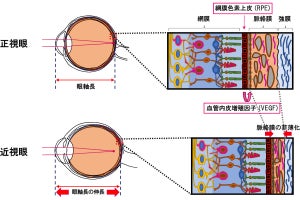
近視進行における強膜小胞体ストレスの関与。(A)正視(正常)眼と近視眼。近視眼の強膜では小胞体ストレスが生じ、それによりコラーゲン遺伝子発現プロファイルの変化やコラーゲン分解促進などが起こることで、強膜の菲薄化や物性の変化が生じる。その結果、眼軸長が伸長し、網膜より前面で焦点を結ぶようになる。(B)近視進行のメカニズム。近視誘導刺激は強膜で小胞体ストレスを惹起し、その下流のPERK、ATF6経路を介して眼軸を伸長する (出所:慶大プレスリリースPDF)
なお、近視は患者数の多さと、視覚障害の危険性を有しているにも関わらず、効果的かつ安全に眼軸伸長を抑制する薬剤は現時点で存在しておらず、研究チームでは、今回の研究で見出した4-PBAは近視の治療を可能とする薬剤の創出につながるものであり、社会的なインパクトが極めて大きいものであると考えられるとしている。