具体的には、今回の研究では、20歳以上の日本人アトピー性皮膚炎患者46名および健常者46名を対象に、DOCK8の全エキソン(48個)におけるゲノム配列をダイレクトDNAシーケンシングによって解読し、比較検討が実施された。その結果、DOCK8エキソン2上に存在する一塩基多型の「rs17673268」がアトピー性皮膚炎患者と健常人の間で大きく異なっていることが明らかにされたとする。
また、DOCK8遺伝子多型において、大半の人ではシトシン(C)塩基だが、アトピー性皮膚炎患者ではチミン(T)塩基に置き換わっている頻度が有意に高いことが確認されたとするほか、両アレルがT(TT遺伝子型)である頻度は健常者11%に対し、アトピー性皮膚炎患者では28%と有意に高くなっており、CC遺伝子型と比べて発症リスクの上昇が示されたという。
さらに、この遺伝子多型とアトピー性皮膚炎の重症度との関連性の解析として、重症度スコアのIGAやEASIを用いたアトピー性皮膚炎患者群での遺伝子多型の比較から、重症の皮膚炎患者(IGAスコア4点)は、CT遺伝子型あるいはTT遺伝子型でしか認められないことが判明したとするほか、中等症以上の患者をEASIスコア(高いほど重症)で比較したところ、CTよりTT遺伝子型でEASIスコアがより高く、重症化している患者が多いことが判明したという。
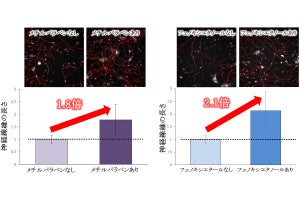
このrs17673268におけるCからTへの一塩基置換は、アラニンからバリンへのアミノ酸置換(ミスセンス変異)をもたらすことから、各々の点変異体を発現させた細胞株を作成し、EPAS1の核移行を調べる実験を実施したところ、TT遺伝子型に該当する遺伝子ベクターを発現した細胞株では、CC遺伝子型に比べてEPAS1の核移行が亢進することが見出されたともする。
-
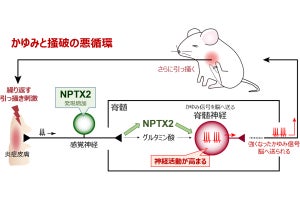
研究成果の概要図。アトピー性皮膚炎、特に重症の皮膚炎患者では、DOCK8のrs17673268部位がTT遺伝子型である頻度が高い。この遺伝子多型は、痒みを引き起こすIL-31の発現を制御する転写因子EPAS1の核移行性に関与している (出所:九大プレスリリースPDF)
研究チームでは、このDOCK8遺伝子多型は機能的な多型であり、EPAS1の核移行を制御してIL-31発現に関与することで、アトピー性皮膚炎の発症や重症化につながっている可能性が示唆されたと説明している。
なお、今回の研究成果は、比較的小規模な人数で得られたものであるため、日本人以外の国籍も含めた、より大規模集団での検討が今後重要になると研究チームではしているほか、この遺伝子多型が、アトピー性皮膚炎患者の抗IL-31受容体抗体への治療反応性予測や層別化医療に応用できる可能性があるとしている。またIL-31はアトピー性皮膚炎だけでなく、結節性痒疹や乾癬、慢性蕁麻疹などの皮膚疾患でも上昇することが報告されていることから、今回のDOCK8遺伝子多型は、これらの皮膚疾患の病態形成にも関与している可能性があるともしている。